-
140
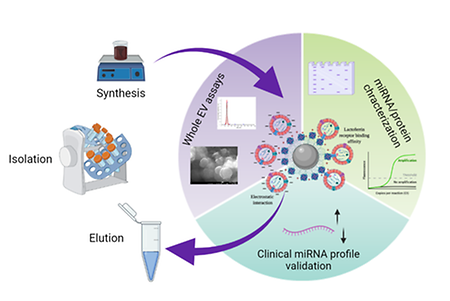
- 연세대 신용 교수팀, 소변 유래 세포 외 소포체를 이용한 전립선암 진단 기술 개발
- < 연세대 신용 교수팀, 소변 유래 세포 외 소포체를 이용한 전립선암 진단 기술 개발 > - 고효율/저비용 세포 외 소포체(엑소좀 포함) 분리 방법 개발 - - 소변에서 세포 외 소포체 유래 miRNAs를 이용한 전립선암 진단법 개발 - - 2월 22일 Journal of Extracellular Vesicles (IF 25.841) 誌 Online 게재 - 연세대학교 신용 교수(생명공학과)는 서울아산병원/울산의대 김청수 교수(비뇨의학과)팀과의 공동연구를 통해 간편한 소변 유래 세포 외 소포체(엑소좀 포함) 분리 기술을 개발하고, 이를 이용해 세포 외 소포체 내 miRNAs를 이용한 전립선암 진단 기술을 개발했다. 전 세계적으로 암세포에서 유래된 세포 외 소포체를 이용한 암 진단 기술이 유망한 분야로 떠오르면서, 혈액 혹은 소변과 같이 비침습적으로 채취가 가능한 액체 생검을 이용한 암 진단 기술이 중요하게 여겨지고 있다. 이에, 임상적으로 사용 가능한 수준으로 액체 생검에서 세포 외 소포체를 빠르고 정확하게 분리할 수 있는 기술 개발의 필요성이 지속적으로 증가하고 있다. 기존에는 세포 외 소포체(엑소좀 포함)를 분리하기 위해 초원심분리기를 이용하거나 소포체의 크기 혹은 표면 장력 등을 이용한 기술들이 사용되고 있으나, 거대한 장비가 필요하거나 시간이 많이 소요되고 비용 대비 분리 효율이 낮아서 실제 임상에서 사용하기에 어려움이 있었다. 연세대 신용 교수 연구팀은 기존 방식의 문제점을 해결하기 위해 새로운 방식(chimeric nanocomposites)의 세포 외 소포체 분리 기술을 개발했다. chimeric nanocomposites는 표면 장력과 물리적 흡착력 및 생체 인식 기술을 접목한 방식으로, 소요 시간이 30분 이내로 기존 대비 적게 소요되며, 소변에서 세포 외 소포체 분리 효율 또한 높인 기술이다. 이에 더해 개발된 기술을 바탕으로 서울아산병원/울산의대 공동연구팀과 협력해, 전립선암 환자의 소변에서 유래된 세포 외 소포체를 분리함으로써 전립선암 환자의 진단에 적용이 가능한지 살펴봤다. 40여 명의 소변 시료에서 세포 외 소포체 유래 miRNAs를 분리해 전립선암 환자와 정상인의 발현 차이를 확인함으로써 개발된 기술을 통해 전립선암 환자를 빠르게 진단할 수 있다는 것을 보였다. 연세대 신용 교수는 “새로운 세포 외 소포체(엑소좀 포함) 분리 기술을 이용하면 기존 기술 대비 간편하고 빠르게 세포 외 소포체 분리가 가능해 환자의 액체 생검을 이용한 진단에 사용하기에 적합하다. 따라서 전립선암을 비롯한 다양한 암 환자의 소변이나 혈액을 이용한 암 진단에 사용 가능하리라 생각된다”며 “더불어, 본 기술이 전립선암 환자의 진단에 임상적으로 실제 사용이 가능한지를 확인하기 위해 더 많은 환자의 소변을 이용해 검증하고자 한다”고 말했다. 본 연구결과는 국제 학술지 ‘세포외소포체저널(Journal of Extracellular Vesicles, IF 25.841)’에 2월 22일 온라인 게재됐으며(제1저자: Thi Thuy Nguyen Dao, 교신저자: 신용 교수, 김청수 교수), 한국연구재단 중견연구자사업, 선도연구센터사업 및 연세대 미래선도연구사업의 일환으로 추진됐다. 논문 제목: Chimeric nanocomposites for the rapid and simple isolation of urinary extracellular vesicles 논문 주소: https://doi.org/10.1002/jev2.12195 (사진 설명) 1. 연구 결과
- 생명공학과 2022.03.03
-
139
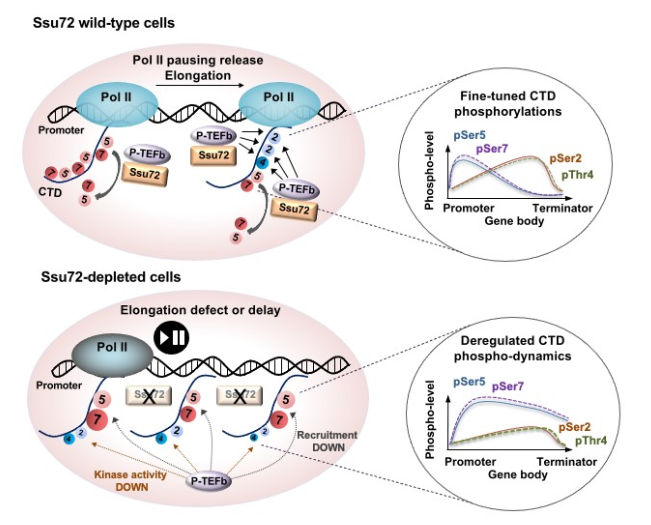
- 신 용 교수 연구팀, 세포 및 조직 특이적 유전자 발현의 ‘새로운 기전’ 규명
- 연세대학교 생명시스템대학 생명공학과 신용 교수 연구팀과 성균관대학교 의과대학 의학과 이창우 교수, 김현수 박사 연구팀은 공동연구를 통하여 포유류 세포 및 조직 특이적 유전자 발현의 새로운 기전을 밝혀내고, 탈인산화효소 Ssu72의 활성이 RNA 중합효소 II(RNA polymerase II 혹은 RNA Pol II)의 전반적인 전사 과정 조절에 핵심인 것을 밝혀냈다. 우리 몸을 구성하는 기관(organ) 및 조직(tissue)들은 다양한 세포들로 이루어져 있으며, 이러한 세포들은 내재되어 있는 그 고유의 특이적인 유전자들의 발현 및 적절한 억제를 통해 세포 항상성을 유지하며, 그 고유한 기능을 유지하고 있다. 특히 임상적으로 다양한 기관 및 조직들의 유전자 발현 조절 실패는 암을 비롯한 여러 대사성 질환, 면역성 질환의 원인임이 잘 알려져 있어서, 탈인산화효소 Ssu72를 통한 세포 및 조직 특이적 유전자 발현 조절은 향후 다양한 인간 질병 치료제 개발에 새로운 전기를 마련할 것으로 사료된다. 연구팀은 본 연구에서 여러 분자생물학, 생화학적 및 생명정보학적 실험방법들을 활용하여 효모에서 부분적으로 알려진 탈인산화효소 Ssu72의 기능을 마우스 조직 안의 다양한 세포들을 이용하여 심도 있게 연구한 결과이다. 이번 연구에서 포유동물의 탈인산화효소 Ssu72는 RNA 중합효소 II 전사 과정 (transcription)의 모든 단계[개시 단계 (initiation step), 전사 신장 단계 (elongation step), 종결 단계 (termination step)]에서 RNA 중합효소 II C-terminal domain (CTD)의 탈 인산화 작용을 통하여 유전자 발현을 조절함을 확인하였다. 또한, Ssu72는 조직 특이적으로 활성화된 유전자들을 우선적으로 통제함을 규명하였고, 이러한 결과들은 Ssu72가 세포내 특이적이고 안정적인 환경을 제공할 수 있는 정교한 유전자 발현기전을 통제하고 있음을 처음으로 밝힌 연구란 점에서 매우 커다란 의의를 갖는다. Mammalian Ssu72 phosphatase preferentially considers tissue-specific actively transcribed gene expression by regulating RNA Pol II transcription. Theranostics (IF 11.556) 2022; 12(1): 186-206.
- 생명공학과 2022.01.13
-
138

- [연구 프론티어] 권호정 교수팀, 인간악성흑색종 단백질 지도 제작
- 권호정 교수팀, 인간악성흑색종 단백질 지도 제작 스웨덴 룬드대학 연구진과 국제협력연구 인간악성흑색종 단백질 지도 제작 통해 악성흑색종 진단 마커 및 치료 가능성 제시 [사진. 권호정 교수(왼쪽), 조지 마르코바가 교수] 생명시스템대학 생명공학과 권호정 교수 연구진은 스웨덴 룬드대학 조지 마르코바가 교수 연구진과 글로벌연구실 국제협력연구를 통해 인간악성흑색종(Malignant melanomas; MM)에 대한 proteomics 및 proteogenomic을 통합한 연구 결과를 두 개의 논문으로 정리해 ‘임상 및 중개 의학(Clinical and Translational Medicine, IF 11.492)’에 발표했다. 두 논문에서는 500개 이상의 악성흑색종 샘플에서 악성흑색종 관련 단백질을 지도화했다(MM500 연구). 딥 러닝 기반 단일 세포 분할 및 proteogenomic 분석법을 적용해 표현형을 분석함으로써 새로운 디지털 흑색종 병리학을 성공적으로 구축했다. MM500 연구에서 질량 분석을 통해 15,500개 이상의 단백질형을 동정했으며, 이들 단백질형 원발성 및 전이성 흑색종 내 염색체 및 세포 내 위치에 대해서도 분류했다. 완성된 분자 지도는 면역 요법 후 조절되는 단백질을 포함한 혈액 단백질 발현 분석을 통해 더욱 보완됐으며, 해당 결과는 현재까지 확인된 인간 전체 단백체의 72%를 포함한다. Human Melanoma Proteome Atlas 구축을 주요 내용으로 하는 두 논문 중 ‘The Human Melanoma Proteome Atlas - Defining the Molecular Pathology’ 논문은 종양이 절제된 해부학적 부위, MM500 코호트의 임상조직병리학적 특징, 샘플의 상세한 조직학적 특징을 제시하고, 분석된 흑색종 종양의 단백질 프로파일을 소개했다. 또한 흑색종 배양 세포주 및 많은 양의 종양 세포 또는 기질이 있는 조직에서 단백질의 차별적 발현뿐만 아니라 염색체 및 세포 위치에 대한 세부 정보를 모두 제시했다. 관련 추가 논문인 ‘The Human Melanoma Proteome Atlas - Complementing the Melanoma Transcriptome’은 미국 NIH 암센터(NCI)의 The Cancer Genome Atlas (TCGA)의 유전적 데이터와 proteomic 분석을 통합했으며, transcriptome, 발현된 단백질, 정량화, 이들의 위치, 돌연변이, splice isoforms 및 PTM 변이에 대해 체계적으로 지도화한 정보를 제공했다. 아울러 TCGA 전사체에서 전사체가 누락된 단백질의 검출, 단백질 수준에서 발현되는 흑색종 유발 돌연변이, 흑색종 환자의 혈장 내 단백질 분석 및 검출에 대해 제시했다. MM500 코호트는 232명의 환자로부터 얻은 294개 종양의 505개 샘플로 구성됐으며, 확인된 15,500개의 proteoform 중 많은 수의 세포질 단백질과 2,000개의 수용체 및 리간드와 같은 막 단백질이 포함됐다. 연구진은 세포 분열, splicing 기전 및 대사에 관련된 단백질들이 매우 높게 발현돼 있음을 발견했으며, 상기 결과를 통해 흑색종에서 미토콘드리아 기능이 중요함을 시사했다. 본 연구에서 제시된 흑색종 프로테옴의 개요, 전사체 및 돌연변이 데이터의 통합, 심층적인 종양의 조직병리학적 특성과의 조합은 인간 악성흑색종양 진단 및 치료의 새로운 근간을 제공할 수 있을 것으로 기대된다. [그림. 분자 수준의 병리학적 분류: 디지털화된 흑색종 조직 샘플(우), deep neural network 방법을 이용한 조직 내 단일 세포 분할(좌). 본 연구결과를 소개한 미국 NIH 암센터(NCI)의 소개 기사(2021.12.10.)] 이번 연구는 9개 국가(한국, 스웨덴, 헝가리, 네덜란드, 오스트리아, 미국, 일본, 중국, 브라질) 연구자가 참여한 국제협력 컨소시엄 연구로 진행됐으며, 권호정 교수는 과학기술정보통신부-한국연구재단이 추진하는 기초연구사업(글로벌연구실사업)의 지원으로 본 과제를 수행했다. 또한 조지 마르코바가 교수는 생명시스템대학 BK21 연세바이오시스템 교육연구단 겸임교수로서 권호정 교수 연구팀의 글로벌연구실사업에 참여해 2015년부터 국제협력연구를 활발히 수행해 왔다. 본 결과가 발표된 ‘Clinical and Translational Medicine(IF 11.492)’은 Wiley지가 발행하는 국제학술지 분야 Q1의 우수학술지이다. 논문정보 ● 논문제목 1. The Human Melanoma Proteome Atlas - Defining the Molecular Pathology 2. The Human Melanoma Proteome Atlas - Complementing the Melanoma Transcriptome ● 논문주소 1. https://doi.org/10.1002/ctm2.473 2. https://doi.org/10.1002/ctm2.451 URL : https://www.yonsei.ac.kr/ocx/news.jsp?mode=view&ar_seq=20211220153238365094&sr_volume=631&list_mode=list&sr_site=S&pager.offset=0&sr_cates=25
- 생명공학과 2021.12.21
