-
128
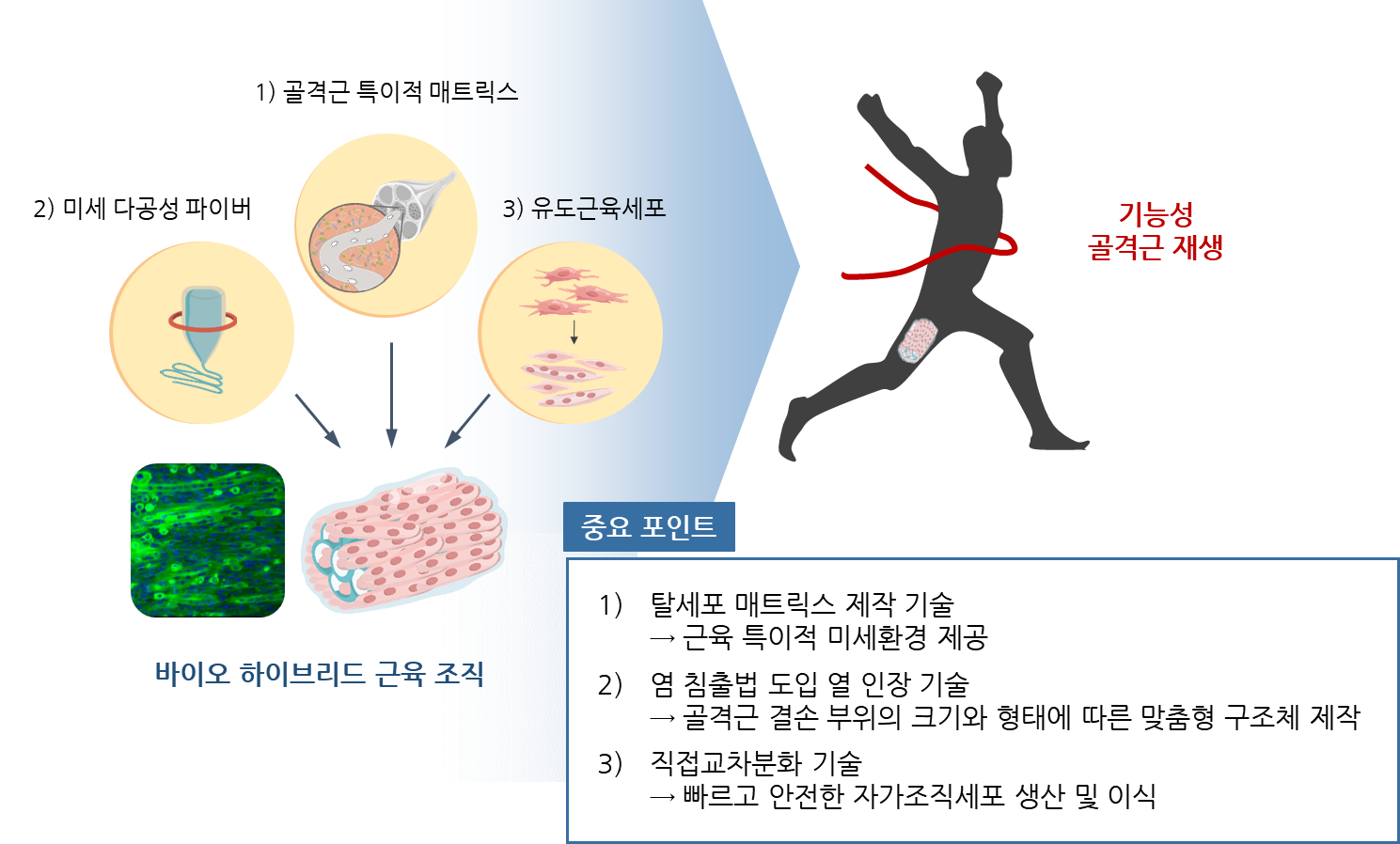
- 조승우 교수 연구팀, 재생의료를 위한 맞춤형 인공 근육 조직 개발
- 연세대학교 생명공학과 조승우 교수 연구팀은 매사추세스 공과대학교 (MIT) PolinaAnikeeva 연구팀과 공동연구를 통해 근육세포 리프로그래밍 기술, 탈세포 매트릭스 제작기술, 미세구조 다공성 파이버 제작기술을 접목하여 근육 질환 치료를 위한 인공 조직을 개발하였다. 연구팀은 먼저 근육 조직 특이적인 생화학적·물리적 미세환경을 조성하기위해 탈세포 (decellularization) 매트릭스를 제작했다.이와 더불어, 열 인장 기술(thermal drawingmethod)과 염 침출법(salt-leaching method)을 이용하여 골격근 결손부위의 형태와 물리적 특성에 따라 다양한 모양과 다공성 구조를 가지도록 맞춤 제작할 수 있는 미세구조 파이버 제작 기술을 개발해 실제 근육의 미세환경과유사한 수준의 인공 근육 지지체를 제작하였다. 이렇게 제작된 인공 근육 지지체는 피부세포를 근육세포로리프로그래밍 하는 직접교차분화 (direct conversion) 효율을 증진시켰으며, 최종적으로 생산된 바이오 하이브리드 근육 조직은 마우스 근육 손상 모델에 이식했을 때, 근육 조직 재생뿐만 아니라 혈관 및 신경 조직 재생까지 유도하여 기능성 근육 조직 재생에 성공할 수 있었다. 개발된 바이오 하이브리드 근육 조직에 사용된 근육 세포는 비교적 채취하기 쉬운 자가 피부세포를 직접교차분화하여제작했기 때문에 기존 세포치료제의 면역거부반응 문제를 해결하였고, 기존 근육 재생 치료보다 월등히 향상된기능성 골격근 재생을 유도하여 임상 적용 가능성을 보여주었다. 이번 연구는 조승우 교수 연구팀의 진윤희 연구교수와 전은제 대학원생이 주저자로 참여하여, 융합 소재 분야 세계 최고 권위의 학술지 중 하나인 AdvancedMaterials (2019년 Impact factor: 27.398) 저널에 게재되었고, 연구 내용의 중요성과 우수성을 인정받아 Advanced Materials 4월호표지 논문으로도 선정되었다 (논문 제목: Functionalskeletal muscle regeneration with thermally drawn porous fibers andreprogrammed muscle progenitors for volumetric muscle injury).
- 생명공학과 2021.04.26
-
127
- 이상규 교수, 교원 창업회사 굳티셀 시리즈B 380억 투자 유치
- 굳티셀은 380억 규모 시리즈B 투자 유치를 마쳤다고 발표했다. 2020년 12월 말 예정인 본사 확장 이전을 완료하고 조절T세포 치료제 연구 인력을 확보하는 데 이 자금을 사용할 계획이다. 굳티셀은 지난 18일까지 납입 받은 350억원과 오는 24일 납입 예정인 30억원을 포함해 모두 380억원을 시리즈B 투자로 유치했다. 투자 기관은 기존 투자자인 스마일게이트인베스트먼트, 포스코기술투자, 아주IB투자와 신규 투자자인 LB인베스트먼트, DS자산운용, 서울투자파트너스, 아이디벤처스, 알바트로스인베스트먼트, 하나벤처스, 유니온투자파트너스 등이다. 굳티셀은 35년간 면역세포의 일종인 T세포에 대해 면역학 연구를 해 온 이상규 연세대 생명공학과 교수가 2016년 세운 세포치료제 개발 기업이다. 이번 투자는 2018년 유한양행에서 50억원 투자를 받은 뒤 이뤄진 두 번째 대규모 자금 유치다. 굳티셀은 유치한 투자자금을 바탕으로 올 연말 서울 마포구 상암동으로 본사를 확장 이전하고 연구 개발 인력을 충원할 계획이다. 이 회사는 2018년 11월 유한양행과 항암 항체치료제 파이프라인 1개에 대해 공동연구 계약을 체결하기도 했다. 주력 연구 분야는 조절T세포 치료제다. 조절T세포는 고형암 및 자가면역질환에서 면역 반응의 균형 유지 역할을 담당하는 면역세포다. 고형암 치료를 위해선 조절T세포의 기능을 낮춰야 하고 자가면역질환에선 그 기능을 높여야 하는 것으로 알려져 있다. 미국 바이오 기업인 길리어드는 조절T세포를 표적으로 하는 면역항암제를 개발하는 티조나테라퓨틱스의 지분 49.9%를 3억달러에 지난 7월 인수하기도 했다. 지난 9월엔 조절T세포 기반 항체치료제 개발사인 자운스테라퓨틱스와 총 계약금 7억5000만달러 규모의 기술이전 계약도 체결했다. 굳티셀도 해외 제약사를 대상으로 조절T세포 파이프라인에 대해 기술이전 계약 논의를 진행 중이다. 회사 관계자는 “조절T세포를 표적으로 하는 항체의 성능을 개량하고 인간 항원을 대상으로 달라붙는 정도를 높이는 절차가 마무리 단계에 있다”며 “내년 상반기 중 후보물질 위탁개발생산(CDMO) 계약을 체결해 비임상시험과 공정개발을 수행하겠다”고 말했다. 관련기사 https://www.hankyung.com/it/article/202012212183i
- 생명공학과 2021.03.10
-
126

- 권호정 교수팀, 비만 개선 활성이 있는 천연 화합물 발견 및 작용 기전 규명
- 권호정 교수팀, 비만 개선 활성이 있는 천연 화합물 발견 및 작용 기전 규명 천연 화합물 라이브러리 658 종을 활용해 오토파지를 유도하는 약물을 고효율 탐색 지방 분해 촉진을 통한 대사 개선 효과 및 표적 기전 규명 [사진: (왼쪽부터)권호정 교수, 김다솔 연구원, 황희윤 연구원] 생명시스템대학 생명공학과 권호정 교수 연구팀(공동 제1저자: 김다솔, 황희윤 통합과정생)은 천연 화합물 라이브러리 658종을 활용해 오토파지를 효과적으로 유도하는 화합물인 캠페라이드(Kaempferide)를 표현형 기반 고효율 탐색법으로 발견했다. 오토파지 조절 이상에 의한 관련 질병으로는 대사 이상, 신경퇴행성 질환, 암, 노화 등이 알려져 있으며, 이러한 질환을 효과적으로 조절하기 위해 오토파지를 조절하는 약물을 발굴하고 그 기전을 규명하는 것이 전 세계적으로 주목받고 있다. 또한, 천연 화합물은 자연계에서 발견되는 살아있는 유기체에 의해 생성되는 물질로서, 화학물질 의약품보다 독성이 적다는 장점으로 바이오 식의약품 개발의 주요 소재로 활용되고 있으나 정확한 작용기전이 규명되지 않은 경우가 많아 신약 개발 등 실제 산업화에 어려움이 되어 왔다. 연구팀은 세포주 및 동물 모델을 통해 식용 및 한의약 식물의 대사산물중 하나인 캠페라이드라는 플라보노이드 기본구조의 천연화합물이 지방세포의 오토파지 유도 활성 및 대사 개선 효능을 발휘함을 발견했다. 나아가 비수식 화합물의 표적 단백질 동정 융합 시스템을 통해 캠페라이드가 세포 내 에너지 생성소 기관인 미토콘드리아에서 단백질 합성 신장 인자(elongation factor)인 TUFM 단백질과 직접적으로 결합함을 확인했으며, TUFM과의 직접적인 결합을 통해 오토파고좀 형성을 촉진하고, 한편으로 활성산소-리소좀 칼슘 방출 유도를 통한 오토파지 유전자 발현을 촉진해 오토파지 유도를 통합적으로 조정하는 기전을 최초로 규명했다(그림 참조). [그림: a) 캠페라이드가 처리된 고지방 식이 유도 비만 마우스의 비만 감소 활성 대표 이미지. b) 캠페라이드의 체중 증량 완화 효능 검증. c) 캠페라이드의 혈당 강하 효능 검증. d) 캠페라이드의 오토파지 유도 및 대사 개선 기전 모식도.] 본 연구를 통해 천연 화합물 캠페라이드가 오토파지 유도를 통해 비만 등의 대사 이상 개선에 효과적인 활성이 있음을 발견하고, 미토콘드리아 TUFM 단백질과의 결합을 통해 대사 조절 활성이 발현될 수 있음을 최초로 규명함으로써 대사 개선 관련 치료제 개발에 활용될 수 있는 새로운 천연 화합물과 표적을 동시에 제시했다. 이번 연구성과는 과학기술정보통신부-한국연구재단이 추진하는 기초연구사업(글로벌연구실사업) 및 유전자동의보감 사업의 지원과 한국기초과학지원연구원 유종신 박사 연구팀(공저자; 김진영, 지은선 박사연구원)의 협력 연구로 수행됐으며, 2021년 1월 4일 ‘커뮤니케이션 바이올로지(Communications Biology, SCI)’에 게재됐다. 본 학술지는 네이처(Nature)지가 발행하는 국제학술지로 분야 Q1의 우수학술지이다. 용어설명 ● 오토파지(Autophagy): 세포 내 구성요소의 파괴와 재활용에 질서를 제공하는 세포 구성성분을 자연적으로 분해하는 파괴 기전. 세포 내 영양분이 부족하거나 외부에서 미생물이 침입했을 때와 같은 스트레스 상황에서 세포 스스로 생존을 위해 내부 단백질을 재활용해 항상성을 유지하는 자가 방어기전. ● TUFM (Mitochondrial elongation factor Tu): 미토콘드리아 내부에 위치한 단백질 합성 신장 인자. 오토파고좀 형성에도 관여함. 논문정보 논문명: Activation of mitochondrial TUFM ameliorates metabolic dysregulation through coordinating autophagy induction 저널명: Communications Biology 키워드: 오토파지(Autophagy), DARTS-LC-MS/MS, TUFM, 비만(Obesity), 대사이상질환 (metabolic syndrome) DOI: 10.1038/s42003-020-01566-0 저자: 권호정 교수(교신저자, 연세대), 김다솔(제1저자, 연세대), 황희윤(제1저자, 연세대), 지은선(공저자, 한국기초과학지원연구원), 김진영(공저자, 한국기초과학지원연구원), 유종신(공저자, 한국기초과학지원연구원)
- 생명공학과 2021.01.07
