-
90

- 김지현 교수, 김기태 박사 등 "대장균 세포공장의 유전체공학과 적응진화 연구에 중요한 진전"
- 김지현 교수, 김기태 박사 등 "대장균 세포공장의 유전체공학과 적응진화 연구에 중요한 진전" 시스템생물학과 김지현 교수와 김기태 박사 등이 합성생물학 기술을 적용하여 대장균에 추가적인 복제개시부위(oriC)를 삽입함으로써 세포의 생장속도와 바이오매스 생산량을 증대시킬 수 있음을 최초로 증명한 결과가 Springer Nature의 BioMed Central (BMC)에서 출판하는 미생물 세포공장 전문 학술지인 Microbial Cell Factories(2021년 IF=6.352)에 “Escherichia coli cell factories with altered chromosomal replication scenarios exhibit accelerated growth and rapid biomass production” 제목으로 게재되었다. 진핵생물과 달리 세균은 염색체당 1개의 복제개시부위를 가지고 있다. 양희진 학생을 포함한 연구팀은 복제개시부위를 대장균의 유전체 내에 추가적으로 삽입하거나 원래 가지고 있는 복제개시부위를 결실시켜 다양한 수의 복제개시부위를 가지는 균주들을 제작하였다. 이후 연구팀은 세포의 염색체 복제 특성과 세포주기를 분석하였고, 그 중 3개의 복제개시부위를 가지는 O3 lacZ dadX 균주가 야생형 모균주에 비해 상대적으로 증대된 생장속도와 바이오매스 생산량을 가지는 것을 확인하였다. 또한, 김기태 박사는 학위논문 연구로 모균주와 O3 lacZ dadX 균주를 조상균주로 활용하여 실험진화 수행과 오믹스 분석을 통해 대장균 집단의 전사체 변화 정도가 집단의 진화적 적응성을 결정할 수 있는 요인으로 작용할 수 있다는 결과를 미국미생물학회(ASM)에서 출판하는 미생물학 분야 온라인 오픈액세스 학술지인 Microbiology Spectrum(2021년 IF=9.043)에 “Transcriptional potential determines the adaptability of Escherichia coli strains with different fitness backgrounds” 제목으로 게재하였다. 연구팀은 야생형 균주와 환경 적합도가 증대된 O3 lacZ dadX 균주를 조상균주로 활용하여 약 2,000 세대 동안의 실험진화를 수행하였으며, 그 결과 이 두 대장균의 환경 적합도가 수렴하는 것을 발견하였다. 이후 진화된 집단의 유전체 서열 분석을 통해 서로 다른 대립 유전자 빈도를 가진 다양한 돌연변이를 규명하였고, 조상균주에 실험진화 과정에서 발생한 돌연변이를 도입했을 때, 초기 환경 적합도가 높은 O3 lacZ dadX 에서 돌연변이의 유익한 효과가 더 낮은 경향이 있다는 것을 확인하였다. 추가적으로 연구팀은 진화된 대장균 집단의 전사체 분석을 통해 유전자 발현량 변화와 유전자 온톨로지 풍부도가 초기 적합도가 낮은 야생형 후손에서 크다는 것을 보여주었고, 전사체의 비유사성이 상대적인 환경 적합도와 비례한다는 것을 최초로 밝혀냈다. 적응진화 과정에서 세균 집단은 여러 돌연변이를 포함하는 세포들이 혼재해 있고, 돌연변이 간에 상위성을 보이며, 역동적인 환경 조건을 가지고 있기 때문에 집단의 적응성을 예측하는 것은 어렵다고 알려져 있다. 그럼에도 불구하고 연구팀은 차세대 염기서열 분석과 대용량 서버를 활용한 서열 데이터 분석을 활용해 유전체 및 전사체 정보를 해독하여 세균 집단의 진화 동역학을 규명하였다. 김지현 교수는 “이 연구는 세균의 진화 궤적이 복잡하고 직관적이지 않을 수 있지만, 전사체의 변화가 세균의 적응성에 주요하게 기여할 수 있다는 것을 입증한 사례로서, 특정 기간 동안의 집단의 적응성은 세균 집단 자체가 가지고 있는 고유한 유전적 능력에 달려 있다는 것을 보여준다.”라고 연구의 의의를 설명했다. 논문정보 ● 논문주소: https://microbialcellfactories.biomedcentral.com/articles/10.1186/s12934-022-01851-z ● 논문주소: https://journals.asm.org/doi/10.1128/spectrum.02528-22
- 시스템생물학과 관리자 2023.01.13
-
89

- 김지현 교수, 허지원 박사 등 “대장암 예후를 예측할 수 있는 장내 미생물 바이오마커 개발”
- 김지현 교수, 허지원 박사 등 “대장암 예후를 예측할 수 있는 장내 미생물 바이오마커 개발” 대변에 존재하는 장내 미생물을 이용해 대장암의 예후를 예측할 수 있다는 사실이 국내 연구진에 의해 최초 규명됐다. 생명시스템대학 시스템생물학과 김지현 교수와 허지원 박사는 서울대 박지원 교수 등과의 공동연구를 통해 대장암 수술 전 환자의 분변에서 수술 후 예후를 예측할 수 있는 장내 미생물들을 찾아내고 이들을 조합한 바이오마커를 개발했다. 연구 성과는 스프링거 네이처(Springer Nature)의 바이오메드 센트럴(BioMed Central, BMC)에서 출판하는 마이크로바이옴 분야 최고 전문 학술지 ‘마이크로바이옴(Microbiome, 2021년 IF=16.837)’에 11월 28일 게재됐으며, 관련 특허도 출원했다. 대장암은 전 세계에서 세 번째로 많이 발생하고 두 번째로 사망률이 높은 암이며, 대장절제술 이후 암이 재발하거나 진행하는 경우가 많아 예후를 미리 예측하는 것이 매우 중요하다. 하지만 현재까지 비침습적으로 대장암의 예후를 예측할 수 있는 미생물 바이오마커 스크리닝은 성공적이지 못했다. 이에 연구진은 대장암 환자 333명의 장내 마이크로바이옴에서 종양절제 후 예후를 예측할 수 있는 균주들을 탐색했다. 기존 연구들은 대부분 한두 개의 병원성 미생물만을 표적해 예후를 분석했으나, 이번 연구에서는 차세대 시퀀싱과 생물정보학 기술을 활용해 광범위한 스크리닝을 진행했다. 대장암 환자에 대한 원발성 종양절제술 전 2주 이내의 대변 샘플을 수집해 차세대 유전자 시퀀싱을 수행하고, 수술 후 대장암 진행 및 감소 여부를 각각 약 3년가량 추적 관찰했다. 인간의 장내 미생물 군집은 프레보텔라(Prevotella) 형과 박테로이데스(Bacteroides) 형 등 두어 타입으로 구분되는데, 이 중 하나의 대표 미생물인 프레보텔라가 많을수록 대장암의 예후가 좋아진다는 사실을 발견했다. 특히 프레보텔라는 채식을 주로 하는 동양권에서 많이 발견되는 미생물로서 이번 연구 결과는 채식과 대장암 예후의 긍정적인 관련성을 뒷받침하는 과학적 증거가 될 수 있다. 반면 대표적인 병원성 미생물인 푸조박테리움(Fusobacterium nucleatum)과 더불어 3종의 새로운 미생물(Alistipes sp., Dialister invisus, Pyramidobacter piscolens)이 존재하는 경우 대장암 예후가 현저히 나빠짐을 확인했다. 연구진은 발견한 5종의 대장암 예후와 연관성이 있는 장내 미생물을 조합해 대장암 예후 예측 능력이 개선된 새로운 미생물 기반의 바이오마커를 개발했다. 이 미생물 기반 바이오마커는 기존에 활용되는 여러 임상 지표들과 비교했을 때 훨씬 더 우수한 예측력을 보였다. 특히 가장 대표적인 대장암 예후 인자인 암 병기에 장내 미생물 바이오마커를 추가했을 때, 예후 예측력이 뚜렷하게 향상되는 것이 확인됐다. 추가적으로 연구진은 참조 미생물 유전체에 기반해 장내 미생물 대사 체계를 추론하는 분석을 진행했고, 미생물에 의한 비타민 B1 생성이 대장암 예후를 개선할 수 있으며, 장내 세포사멸 면역세포(CD8+ T세포)의 숫자와 높은 양의 상관관계를 보인다는 것을 발견했다. 김지현 교수는 “대장암 예후에 활용될 수 있는 장내 미생물 및 이 미생물들의 대사에 대한 추가 연구를 통해 미생물을 이용한 대장암 예후 개선과 재발 방지의 가능성이 열렸다.”고 말했으며, 허지원 박사는 “이번 연구결과의 후속으로 식이와 장내 미생물 대사가 대장암 예후에 미치는 영향과 이들의 관계를 규명하는 연구를 추진할 것”이라고 전했다. 이번 연구는 한국암연구재단과 한국연구재단(바이오‧의료기술개발사업, 다부처 국가생명연구자원 선진화사업) 및 연세 시그니처 연구클러스터사업의 지원으로 수행됐다. 논문정보 ● 논문제목: Enterotypical Prevotella and three novel bacterial biomarkers in preoperative stool predict clinical outcome of colorectal cancer ● 논문주소: https://microbiomejournal.biomedcentral.com/articles/10.1186/s40168-022-01388-8 ● 관련 영상: https://youtu.be/pIrXB2CvXcA
- 시스템생물학과 관리자 2023.01.02
-
88

- 박재효-조예람 학생, '농식품 R&D Young Creator' 우수상 수상
- 박재효-조예람 학생, '농식품 R&D Young Creator' 우수상 수상 농림식품기술기획평가원(이하 농기평)은 12월 15일 '2022년 농식품 R&D Young Creator' 공모전 수상자를 선정·발표했다. 이번 공모전은 지난 9월 1일부터 22일까지 농식품 산업에 관심 있는 대학원생을 대상으로 연구과제 제안서를 접수했다. 총 21개 팀의 제안서 중 12개를 채택해 약 43일 동안 기획연구활동을 지원했고, 최종 심사 결과 최우수상 1점, 우수상 2점, 장려상 3점을 선정했다. 박재효-조예람 학생의 '마이크로바이옴 비너스' 팀의 '유전체 편집 기술을 이용한 작물 마이크로바이옴 제어 및 합성 연구'는 우수상을 수상했다. 이번 공모전은 참가자들이 직접 연구 아이디어를 기획하고, 연구개발계획서를 작성하는 등 연구자로서 한 단계 도약할 수 있는 좋은 기회였다는 평이 주를 이뤘다. 이에 농기평에서는 지속적으로 공모전을 추진해 농식품 R&D Young Creator의 성장을 도울 예정이다. 출처: https://www.thekpm.com/news/articleView.html?idxno=140850
- 시스템생물학과 관리자 2023.01.02
-
87

- 김지현 교수 대통령표창…농축산과학기술대상 시상식
- 김지현 교수 대통령표창…농축산과학기술대상 시상식 농림축산식품부는 28일 열리는 ‘제25회 농림축산식품 과학기술대상 시상식’에서 김지현 연세대학교 교수에 대한 대통령 표창 시상을 진행한다고 27일 밝혔다. 김지현 교수는 농식품 유용 미생물 유전체 정보를 활용하여 발효식품 종균(김치류, 주류, 발효유), 작물·동물의 미생물제제, 건강기능식품 등 바이오소재 산업 발전에 기여했다는 평가를 받았다. 정황근 농식품부 장관은 “기후변화, 세계 경제의 불확실성 등 어려운 여건을 맞아 미래 농업과 식품산업의 발전을 위해 과학기술계의 역할이 더욱 중요해졌다”며 “정부도 과학기술과 산업발전을 위해 최선을 다하겠다”고 말했다. 출처: https://biz.chosun.com/policy/policy_sub/2022/11/27/TB43GAAFWBFAFB5WYS7Q7N4PJI/
- 시스템생물학과 관리자 2022.12.07
-
86
- 배현숙 교수, 한국식물학회 최우수 학술상 수상
- [배현숙 교수, 한국식물학회 최우수 학술상 수상] 생명시스템대학 시스템생물학과 배현숙 교수는 2022년 11월 9일 개최된 사단법인 한국식물학회에서 주관하는 2022년도 한국식물학회 정기학술대회에서 우수한 연구업적과 활발한 학회 활동으로 학회 발전에 크게 기여한 공로를 인정받아 최우수학술상을 수상했다.
- 시스템생물학과 관리자 2022.12.07
-
85
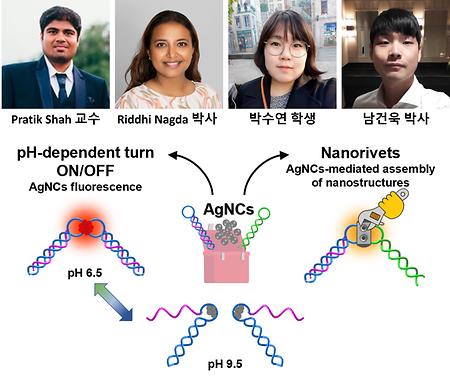
- 양성욱 교수, 노영훈 교수 공동 연구팀, 은나노클러스터(AgNCs)의 Hoogsteen 삼중 DNA 구조와 hairpin-loop DNA 구조를 연결하는 형광 리벳 기능 규명
- 양성욱 교수, 노영훈 교수 공동 연구팀, 은나노클러스터(AgNCs)의 Hoogsteen 삼중 DNA 구조와 hairpin-loop DNA 구조를 연결하는 형광 리벳 기능 규명 시스템생물학과 양성욱 교수 연구팀과 생명공학과의 노영훈 교수 연구팀은 공동 연구를 통해 은나노클러스터(AgNCs)의 Hoogsteen 삼중 DNA 구조와 hairpin-loop DNA 구조를 연결하는 형광 리벳 기능을 규명하였다. 본 연구는 그 우수성을 인정받아 ACS Nano 온라인판에 2022년 8월에 게재되었다. (Silver Nanoclusters Serve as Fluorescent Rivets Linking Hoogsteen Triplex DNA and Hairpin-Loop DNA Structures. ACS Nano(IF=18.2). 2022 Aug 11. doi.org/10.1021/acsnano.2c06631). 리디 나그다 박사 (제 1 저자), 박수연 학생(제 1 저자), 원자력 연구원의 정일래 박사 (제 1 저자), 남건욱 박사 (제 1 저자), 연세대의 하리 찬다나 야다발리, 김영민, 양경직 학생, 고려대의 강주연 박사, 조민행 교수, 덴마크 코펜하겐 대학교의 모튼 비어럼 교수연구팀 , 피터 터스럽 교수가 공동저자로 덴마크 로스킬데 대학교의 프라틱샤 교수, 전북대의 김태환교수가 공동 교신저자로 참여하였음. 기존 연구에서는 hairpin, duplex 같은 DNA 2차 구조가 여러 색상의 형광 은나노클러스터를 loop 구조 외부에 형성시킬 수 있음을 입증하였다. 본 연구는 이러한 기존 연구를 바탕으로 Hoogsteen 삼중 구조에서의 형광 은나노클러스터의 성질을 규명하였음. 그 결과, 훅스텐 삼중 DNA 구조에 클러스터링된 은나노클러스터의 적색 형광은 pH 변화에 따라 켜고 끌 수 있음을 확인할 수 있었다. 이에 더해, 은나노클러스터가 DNA 삼중 구조와 hairpin 구조 사이에서 리벳으로 작용, 이형 이량체 구조를 매개할 수 있음을 확인하였고, 이러한 구조적인 다변성에 따라 오렌지색 형광이 발생함을 확인하였다. 이 결과를 바탕으로 왓슨-크릭 결합 외의 비정형적인 DNA origami의 가능성을 제시하였다. 비정형적인 상호작용은 DNA origami에 다른 나노 화학 물질의 추가적인 결합 가능성을 제시할 수 있으며, 이를 바탕으로 다양한 3차원 나노 소재 생성에 기여할 수 있을 것으로 기대한다.
- 시스템생물학과 관리자 2022.08.25
-
84
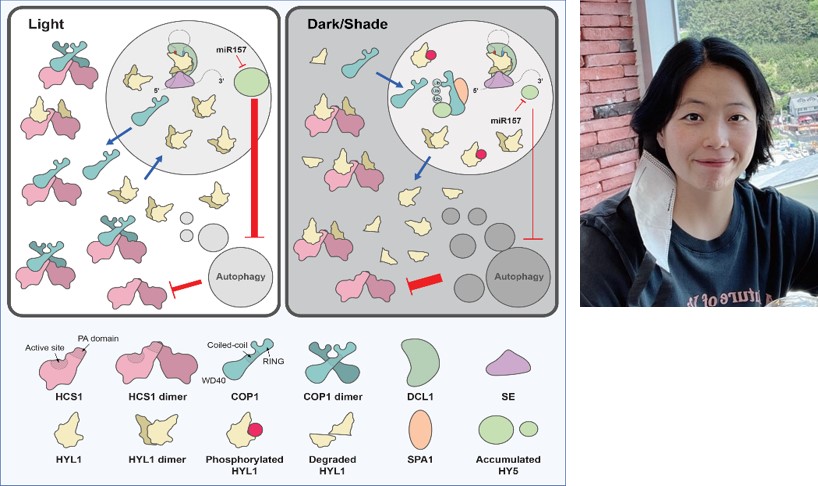
- 양성욱 교수 연구팀 “낮과 밤의 전환에 따라 식물의 miRNA 생합성을 억제하는 프로테이즈 동정하고 그 기능을 최초로 규명”
- 양성욱 교수 연구팀 “낮과 밤의 전환에 따라 식물의 miRNA 생합성을 억제하는 프로테이즈 동정하고 그 기능을 최초로 규명” 본 연구팀은 낮과 밤이 전환되는 과정에서 식물의 miRNA 생합성을 억제하는 프로테이즈를 최초로 규명했다. 이 연구는 PNAS (Proc. Natl. Acad. Sci. USA) 논문에 2022년 2월 게재됐었다 (“HYL1-CLEAVAGE SUBTILASE 1 (HCS1) suppresses miRNA biogenesis in response to light-to-dark transition.” PNAS (2022) doi.org/10.1073/pnas.2116757119) 현재까지 miRNA 생합성 과정에 관여하는 주요 프로세서 단백질들의 기능에 대해 잘 알려져 있지만 단백질들의 조절, 특히 분해조절 기작에 대한 연구는 굉장히 미흡한 상태였다. 광상태에 비해 암상태에서 HYL1 단백질 수준이 굉장히 낮아지게 되는데, 이때 광신호 조절에 중요한 유전자인 COP1 E3 ligase가 관여하게 된다. 본 연구에서 세포질 단백질인 HCS1(HYL1-Cleavage Subtilase 1) 프로테이즈를 동정하였고, HCS1가 HYL1 단백질에 직접 결합하여 분해를 조절하는 것을 밝혔다. 또한 HCS1은 COP1 단백질과 결합하여 세포질의 HYL1 단백질 분해를 억제하게 된다. 빛에 따른 COP1-HCS1결합의 유무를 통해 HYL1 단백질 수준을 조정하여 miRNA 생합성 과정이 조절되는 새로운 메커니즘을 제시하였다. 본 연구는 정현주 연구교수가 주도하였고, 최석원 박사가 참여하였고, 제주대학교 부경환박사, 제노헬릭스의 조석근박사의 공동 연구로 진행되었다. 참여저자: 김지은, 오영경 학생, 한민균 학생, 유문영 박사, 이창우 박사, 크리스천 뮬러 학생, 프라틱 샤 박사, 김구민 학생, 양우림 박사
- 시스템생물학과 관리자 2022.02.17
-
83
- 연세대-경상국립대 연구팀, "헬리코박터만 위 질환을 유발하는 것이 아니다"
- 연세대-경상국립대 연구팀, "헬리코박터만 위 질환을 유발하는 것이 아니다" 위 질환이 있는 사람의 위강내 미생물을 이식받은 무균 마우스에서 위암 전단계에 보이는 전암성 병변이 나타나 주목받고 있다. 한국연구재단은 이용찬, 남기택, 김지현 교수(연세대학교) 연구팀이 경상국립대학교 권순경 교수와의 공동연구를 통해 위 질환환자의 위강내 미생물에 의한 마우스에서의 위 질환 유도에 성공했다고 밝혔다. 사람과 유사한 위강 미생물 환경을 보유한 새 동물모델을 구축, 마이크로바이옴(microbiome)과 인체 위 질환의 상관관계를 밝히는데 귀중한 재료가 될 것으로 기대된다. 연구팀은 사람의 위 조직 혹은 위액을 토대로 위강내 전체 미생물군집을 무균 마우스에 이식하여 사람의 위강 마이크로바이옴과 유사한 마우스 모델을 얻는데 성공했다. 장상피화생 또는 위암이 있는 환자의 위강 내 미생물군집을 이식받은 무균 마우스 위 점막에서 염증과 전암 병소인 장상피화생이 높은 비율로 관찰되었다. 또한, 1년 장기추적한 결과, 이들 무균마우스에서 높은 비율로 전암성 병변인 이형성이 진행된 현상을 관찰하였다. 나아가 연구진은 병변 유발에 관여하는 미생물을 추적하고자 사람과 마우스의 미생물군집 정보를 비교 분석하였다. 그 결과 인체 미생물군집이 마우스에 선택적으로 정착하며, 이식 받은 무균 마우스의 위 조직에 헤모필루스, 게멜라, 베일로넬라 속 세균이 상대적으로 많이 존재하는 반면 아커만시아와 박테로이즈 속 세균은 적다는 것을 알아냈다. 한편 헬리코박터 파일로리는 환자의 위에 높은 비율로 존재함에도 불구하고 이식받은 무균 마우스의 위 조직에서는 관찰되지 않았다. 헬리코박터 파일로리 뿐만 아니라 위 속 다른 미생물도 위암 등 위 질환을 유발할 수 있음을 보여준 셈이다. 이용찬 교수는 “분변 샘플을 재료로 하는 대장 마이크로바이옴에 비해 위강 마이크로바이옴에 대한 논문은 상대적으로 적다”면서 “우리나라의 높은 위암 발병률을 고려할 때 이번에 구축된 마우스 모델이 위 질환 원인 미생물 규명에 도움이 될 것”이라고 설명했다. 위암화 과정을 동물모델에서 직접 구현한 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오·의료기술개발사업 등의 지원으로 수행되었으며 연구결과는 거트(Gut)에 2021. 8월 13일(온라인) 발표되었다. 논문명 : Human gastric microbiota transplantation recapitulates premalignant lesions in germ-free mice 저널명 : Gut (2020 JCR IF = 23.059) 출처: [BRIC Bio통신원] 헬리코박터만 위 질환을 유발하는 것이 아니다 ( https://www.ibric.org/myboard/read.php?Board=news&id=334492 )
- 시스템생물학과 관리자 2022.01.16
-
82
- 배현숙 교수 연구팀 "엽록체와 내막계에 위치하며 POR와 BR 수용체 BRI1을 기질로 결합하는 DAY 샤페론의 식물의 빛 성장 (photomorphogenesis) 조절 메커니즘 분석 "
- 엽록체와 내막계에 위치하며 POR와 BR 수용체 BRI1을 기질로 결합하는 DAY 샤페론의 식물의 빛 성장 (photomorphogenesis) 조절 메커니즘 분석 본 연구실은 CPP1 엽록체 샤페론의 엽록소 생합성 효소 POR를 보호하는 기작을 밝혀 2013년 Plant Cell에 발표하였다. 이번 논문은 CPP1 논문의 후속으로 CPP1의 homolog인 CPP2/DAY 샤페론의 기능을 규명하였다. 엽록체와 내막계에 위치하며 POR와 BR (Brassinosteroid) 수용체 BRI1을 기질로 결합하며 보호하는 DAY 샤페론의 식물의 빛 성장 (photomorphogenesis) 조절 메커니즘을 분석하였다. DAY 샤페론은 식물의 초기 빛 성장의 핵심인 엽록체 발달과 BR 신호전달을 동시에 조절하는 매우 중요한 식물 생장조절 인자이다. 또한 최근 BR 신호전달의 하위인자인 BZR transcription factor와 BIN2 kinase가 TOR 신호전달의 downstream effector로 작용한다는 것이 발표되었다. DAY는 엽록체에도 존재하지만 내막계에도 위치하며 엽록소 생합성 효소인 POR와 BR receptor BRI1의 샤페론으로 작용함. DAY 단백질끼리의 상호작용을 BiFC와 co-IP를 이용하여 분석하였으며 이 상호작용은 엽록체와 내막계에서 동시에 일어난다. 또한 DAY 유전자가 RNAi기법으로 silencing 되었을 때 BRI1 receptor의 subcellular localization을 pBRI1::BRI1-GFP line과 cross하여 분석하였는데 정상조건에서는 BRI1은 애기장대 뿌리세포의 세포막에 위치하고 있는데 DAY가 결핍되면 GFP signal이 줄어들면서 세포의 내부에서 주로 발견된다. Yeast two hybrid을 이용하여 DAY가 BRI1의 cytosolic kinase domain과 아주 강하게 결합하는 것을 밝혔다. DAY 샤페론은 식물 빛 성장의 핵심인 엽록체 발달과 BR 신호전달을 동시에 조절하는 매우 중요한 식물 생장조절 인자이다. Chaperone-like protein DAY plays critical roles in photomorphogenesis. Nature Communications 12, 4194. 이호석, 최일영, 전영, 인희경, 조희경, 김지우, 김재희, 이정민, 이성희, Julian Bünting, 서동혜, 이탁, 이두화, 이인석, 오만호, 김태욱, Youssef Belkhadir*, 배현숙* (co-corresponding author) (2021)
- 시스템생물학과 관리자 2021.12.28
-
81

- 김지현 교수, 정유숙 학생 등 "합성생물학 적용 대장암 치료제 마이크로바이옴에 효과 발견"
- 21.05.13 합성생물학 적용 대장암 치료제 마이크로바이옴에 효과 발견 시스템생물학과 김지현 교수와 정유숙 박사과정 학생이 (주)쎌바이오텍과의 공동연구를 통해 합성생물학 기술을 적용하여 대장암 치료 단백질 P8을 탑재한 프로바이오틱스가 장내 마이크로바이옴을 조절하여 장내 미생물 불균형을 완화하고 유익균의 증가와 유해균의 감소를 초래하는 것을 최초로 발견한 결과가 Springer Nature의 BioMed Central (BMC)에서 출판하는 최고의 마이크로바이옴 전문 학술지인 Microbiome에 “A synthetic probiotic engineered for colorectal cancer therapy modulates gut microbiota” 제목으로 게재됐다. 연구팀은 김치에서 분리한 토종 프로바이오틱스인 페디오코커스 펜토사세우스(Pediococcus pentosaceus) SL4 균주를 이용하여 치료용 단백질인 P8을 분비하는 시스템인 PP*-P8를 개발하였으며 이를 이종이식 종양 및 염증성 대장암 마우스 모델에 투여했을 때 우수한 항암 효과를 보인다는 것을 증명하였다. 또한 염증성 대장암 마우스 모델의 마이크로바이오타를 2개월 동안 추적한 결과 PP*-P8을 투여하는 동안 유익균인 아커만시아(Akkermansia)가 증가하고 유해균인 튜리시박터(Turicibacter)가 감소하였으며 장내 불균형이 완화되는 등 항암 효과와 더불어 장내 마이크로바이옴 조절 효과도 있다는 것을 규명하였다. 아커만시아는 최근 여러 대사 질환에 예방 또는 치료 효과를 보여 차세대 프로바이오틱스로 각광받고 있는 균주이다. 일반적으로 대장암 치료에 사용되는 항암 화학요법은 암세포뿐만 아니라 빠르게 분열하는 정상세포에도 작용하기 때문에 위장관계 부작용이나 골수 기능 저하 등 다양한 부작용을 유발한다. 또한 화학요법 중 발생하는 항암제 내성 현상은 대장암 사망률의 가장 큰 원인으로 꼽히고 있으며 장내 미생물이 치료 효과에 큰 영향을 미친다고 알려져 왔다. 그렇기 때문에 최근 들어 마이크로바이옴 기반의 치료제에 많은 관심이 집중되고 있는 상황이지만, 기존에 개발되어 왔던 표적 미생물 항암제는 살모넬라, 리스테리아, 클로스트리디움 등과 같은 병원 미생물 중심으로 연구가 진행되어 왔기 때문에 안전성에 취약하다는 한계가 있었다. 연세대-쎌바이오텍 공동연구팀은 치료용 단백질인 P8을 분비하는 합성 프로바이오틱스 균주 PP*-P8을 통해 효과적으로 대장암을 치료할 수 있을 뿐만 아니라 장내 마이크로바이옴에 긍정적으로 작용함으로써, 화학요법의 부작용과 항암제 내성을 완화시킬 수 있는 미생물 기반 항암 치료제의 효과를 처음으로 규명한 연구라는 점에서 의의가 있다. 마이크로바이오타 분석과 실험적 검증을 주도한 제1저자 정유숙 박사과정 학생은 “이번 연구에서 밝혀진 PP*-P8의 항암 및 장내 미생물 조절 효과는 합성 미생물 기반 마이크로바이옴 신약의 가능성을 입증한 사례로써, 향후 기존 항암 화학요법의 한계를 보완할 수 있는 새로운 개념의 바이오치료제 개발에 활용될 수 있을 것”이라고 연구의 의의를 제시했다. 이번 성과에 대해 김지현 교수는 “한국인의 대장암 발생률은 세계 2위이다. 미생물 신약은 독성이 강한 화학요법에 비해 부작용이 적고 항암효과도 우수할 뿐만 아니라 무너진 장내 환경 개선도 가능하다. 부작용과 재발 가능성이 적은 항암 치료제를 개발하는 데 도움이 되기를 바란다.”고 밝혔다.
- 시스템생물학과 관리자 2021.12.28




